Cellule Dendritiche regolatorie nella prevenzione del rigetto di organo
Abstract
Una delle problematiche più importanti nel trapianto è il rigetto di organo da parte del sistema immunitario. Infatti, la terapia immunosoppressiva (IST) viene somministrata a vita al ricevente, ma è associata a molti effetti collaterali. A tale riguardo si comprende l’importanza di esplorare risorse alternative, basate per esempio su terapie cellulari come l’uso delle Cellule Dendritiche Tollerogeniche (Tol-DCs) ideate per sospendere anticipatamente la IST.
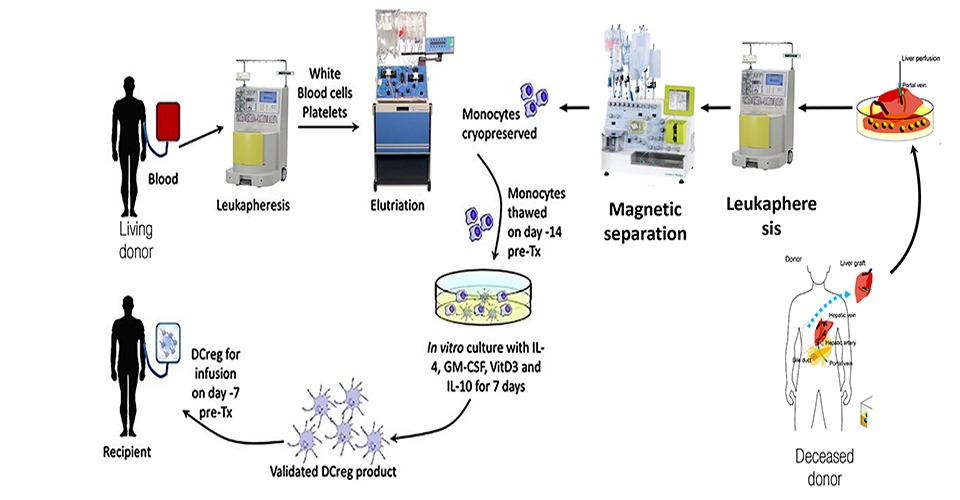
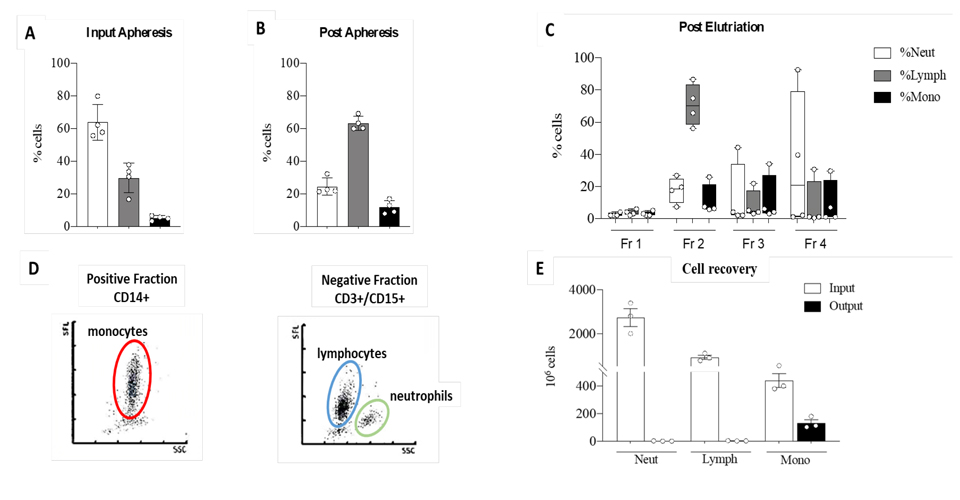
Lo scopo di questo progetto è ottimizzare una terapia cellulare mediate da Tol-DCs per indurre tolleranza immunitaria operativa. Le Tol-DCs vengono ottenute a partire dal prodotto cellulare di perfusione del fegato resecato dal donatore cadavere. Durante l’espianto di fegato dal donatore cadavere a cuore battente, la aorta viene chiusa ed il fegato perfuso attraverso la vena epatica. Il perfusato epatico così ottenuto è normalmente smaltito. Tuttavia, il perfusato rappresenta una risorsa cellulare importantissima, contenente un elevato numero di cellule circolanti nel sangue da/verso i tessuti, tra le quali i precursori delle DCs. Questi precursori, i monociti CD14+ messi in coltura per 7 giorni con fattori di crescita IL4/GM-CSF/IL-10 e Vitamin-D3 danno origine alle Tol-DCs, con elevato potenziale immuno-tollerogenico nei confronti di linfociti T eterologhi.
Impatto:
I pazienti soggetti a trapianto di organo ricevono IST per il resto della loro vita. La IST è associata ad effetti collaterali debilitanti come tumori, infezioni, diabete, malattie cardiovascolari e insufficienza renale. Nel trapianto di organo, la forma ideale di immunosoppressione è quella specifica per il donatore, senza intaccare le difese immunitarie del ricevente né incrementare la suscettibilità ad infezioni di varia natura. Le Cellule Dendritiche, se opportunamente condizionate, possono esser utili allo scopo in quanto in grado di indurre tolleranza nelle cellule del ricevente verso gli antigeni dell’organo del donatore, le quali diventano ipo-responsive verso gli allo-antigeni sviluppando memoria immunitaria.
Le DCreg funzionalmente prevengono il rigetto di organo e permettono lo svezzamento anticipato del ricevente dalla IST.
Il trial in Fase I/II in atto a Pittsburgh presso il gruppo di Angus W Thomsom consiste proprio nella somministrazione di DCreg in pazienti riceventi fegato da donatore vivente. Le DCreg sono ottenute dal prodotto di aferesi del donatore vivente. La frequenza di trapianti di fegato da donatore vivente è però piuttosto inferiore rispetto alla donazione da cadavere. La possibilità di applicare il protocollo delle Tol-DCs anche alla coorte di riceventi di organo da donatore cadavere aumenterebbe notevolmente la casistica, rendendo il trial a più ampio spettro.
La scelta del trapianto di fegato è promettente in quanto il fegato è un organo tollerogenico per definizione ma bene si adatta anche ad altri tipi di trapianto di organo soldo come il rene.
Pipeline
-
CLINICAL
NEED -
DISEASES
ANALYSIS - DISCOVERY
-
PRECLINICAL
VALIDATION -
PRECLINICAL
DEVELOPMENT -
CLINICAL
STUDIES
Principal Investigator
Contatto
Aree terapeutiche:
Prodotto:
ATMP (Advanced Therapy Medicinal Products)
Collaborazioni:
- Thomas E. Starzl Transplantation Institute, University of Pittsburgh, USA
Scarica il pdf del progetto